Paso 7: La educación parte
Si usted está no sólo interesado en la construcción de un generador de hidrógeno, sino también en el fondo de la química, por favor lea esta parte del instructable.
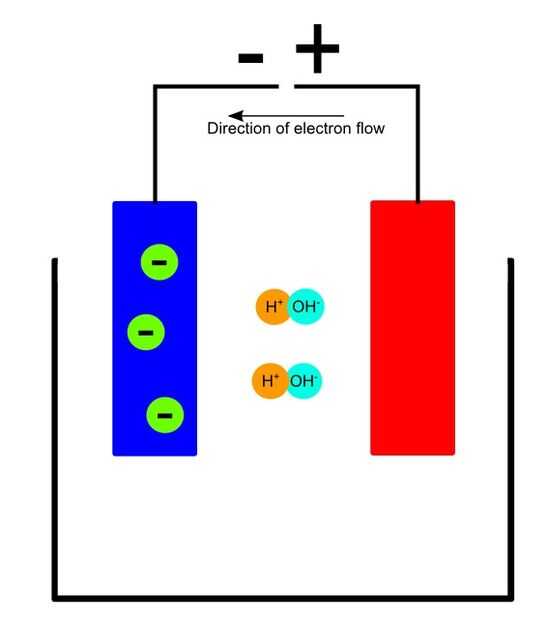
Electrólisis: Electrólisis es una reacción endotérmica. Esto significa que la reacción sólo se ejecuta si agregar energía al sistema. Esto se logra con nuestra fuente de alimentación de CC. El suministro de energía los electrones en el ánodo tira y empuja al cátodo.
Los electrones son de las moléculas de agua. La alimentación de las fuerzas de las moléculas de agua (HHO) para dividir en un Ion hidrógeno cargado positivo (H +) y negativo cargado iones de hidróxido (OH-).
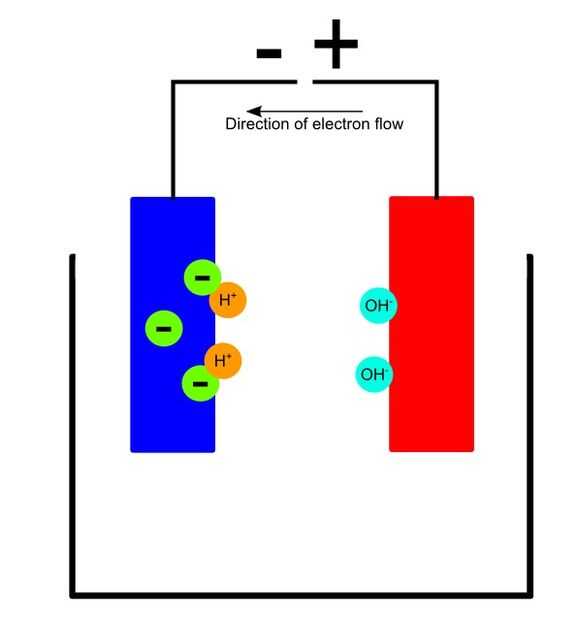
Debido a fuerzas electromagnéticas se tiró de los iones de hidrógeno positivo cargado hacia el cátodo y los iones hidróxido se tiran hacia el ánodo.
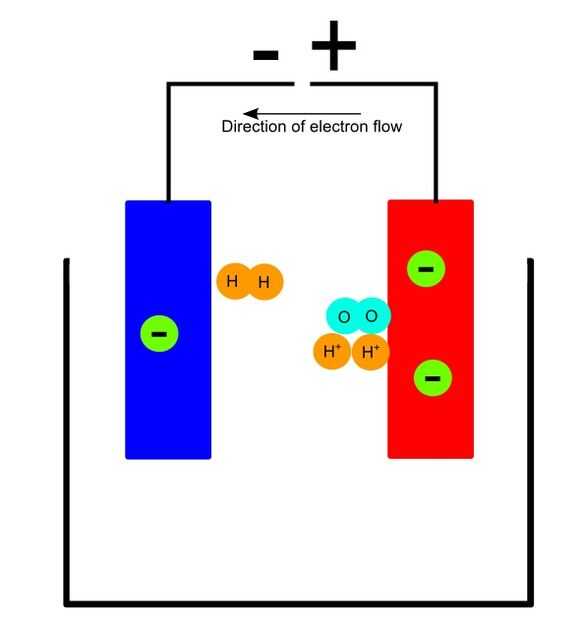
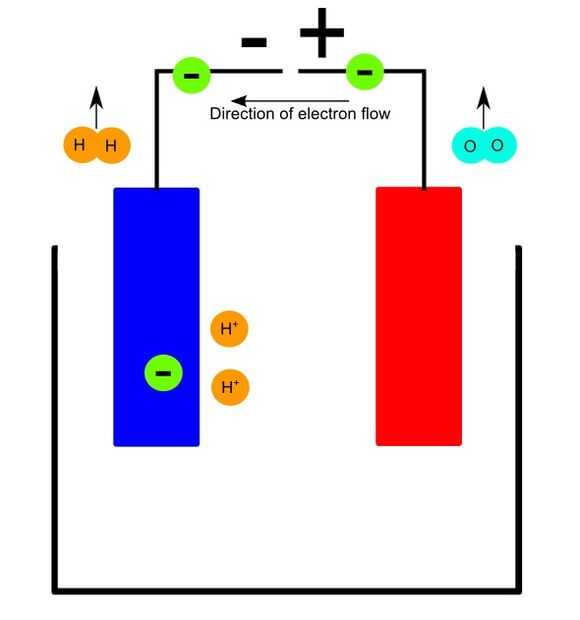
Como electrones a los iones de hidrógeno por el cátodo, los iones de hidrógeno se convierten en hidrógeno (HH).
Porque el ánodo jala electrones, toma los electrones de los iones de hidróxido y los iones hidróxido se convierten en iones de hidrógeno y gas oxígeno (OO). Los iones de hidrógeno luego viaja al cátodo.
¿Por qué utilizamos lapiz como el ánodo?: Utilizamos lapiz como ánodos, porque los metales (excepto platino) se oxidan debido a las reacciones electroquímicas en el envase. Eso significa que si utilizas un ánodo de hierro que básicamente moho lejos mientras que produce hidrógeno. Lo mismo sucede cuando se utiliza cobre. El cobre se transforma en óxido de cobre. Esto ralentiza la producción de hidrógeno y da al agua un color malo.











